Conocimientos previos:
- Célula
- Organelos
- Eucariotas y Procariotas
Introducción
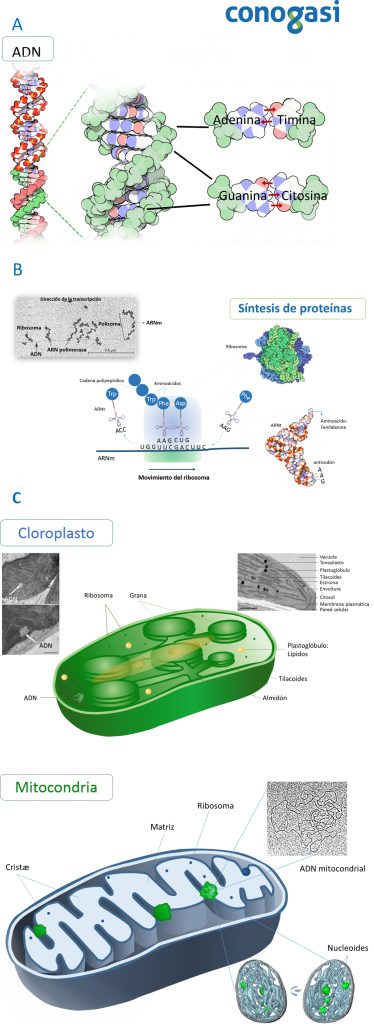
El ADN, o ácido desoxirribonucleico, es el material genético que se encuentra en las células de todos los organismos. Está compuesto por nucleótidos unidos entre sí (Adenina, Timina, Guanina, Citosina) (figura 1A). El ordenamiento y secuencia de los nucleótidos forma un polímero de ADN de doble cadena, el cual se traduce en un ARN mensajero (ARNm), este ARN contiene la información para generar una o varias proteínas utilizando diversos ARNs como intermediarios como los ARN de transferencia (ARNt) y ARN ribosomales (ARNr) (figura 1B). En células eucariotas la mayor parte del ADN se localiza en el núcleo que está rodeada por una bicapa lipídica. Sin embargo, una pequeña cantidad de ADN también se puede encontrar en otras estructuras celulares, como en la mitocondria en animales o cloroplastos en plantas (figura 1C) (A. Checa, 2016).
Gregor Mendel: leyes de la herencia
Antes del descubrimiento de la molécula de ADN, un monje que estudiaba diferentes aspectos de los chicharos llamado Gregor Mendel sentó las bases de las leyes de la herencia genética. Efectuó cruzas entre chicharos con diferentes características (color de la flor, textura de la semilla, etc) y en sus resultados pudo postular las siguentes leyes (Fraser, 2001).
Leyes de Mendel:
- Cuando se cruzan dos variedades puras de una misma especie, los descendientes son todos iguales.
- Al cruzar entre sí los híbridos de la segunda generación, los descendientes se dividen en cuatro partes, de las cuales tres heredan el llamado carácter dominante y una el recesivo.
- En el caso de que las dos variedades de partida difieran entre sí en dos o más caracteres, cada uno de ellos se transmite con independencia de los demás (Fraser, 2001).
El trabajo de Gregor Mendel no fue reconocido cuando lo publicó y no fue sino hasta el año 1900 con los trabajos de Carl Correns, Hugo de Vries y Erich von Tschermak, que se le dio el crédito que merecía su labor y descubrimiento. Los avances científicos posteriores pusieron de manifiesto que las leyes de la herencia de Mendel constituyen una simplificación de procesos que a menudo son mucho más complejos. Sin embargo, estas leyes sirven todavía como base fundamental para la genética moderna (Dahm, 2008).
Los primeros hallazgos del ADN
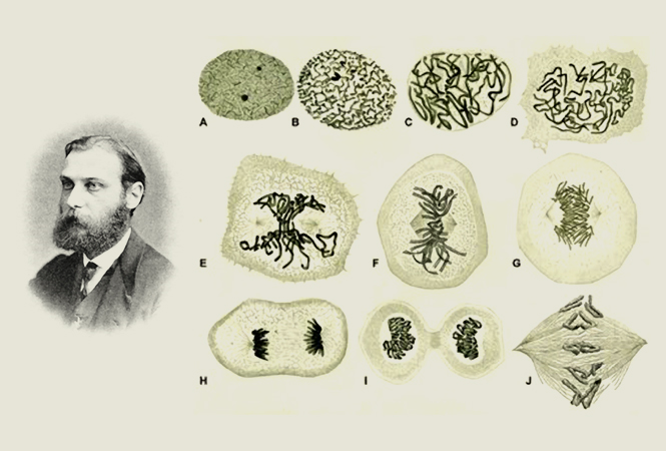
El perfil de ADN, es una técnica que analiza los atributos únicos del ADN de una persona. La aplicación de los perfiles de ADN ha revolucionado las pruebas de maternidad/paternidad, la medicina forense y la identificación de víctimas en desastres. El término “huellas dactilares de ADN” fue acuñado para aludir al uso tradicional de huellas dactilares como medio de identificación humana. Las huellas dactilares clásicas están sujetas a interpretación y las muestras utilizables pueden ser difíciles de obtener. Cuando se lleva a cabo correctamente, las pruebas basadas en el ADN no sóloPosterior a las leyes propuestas por Mendel se dieron los primeros experimentos para descubrir la molécula del ADN. Esto inició con los trabajos del biólogo suizo Johan Friedrich Miescher en 1869, el cual aisló varias moléculas ricas en fosfatos de muestras de pus recuperadas a partir de los vendajes de pacientes. A estos aislados ricos en fosfatos provenientes de los núcleos de las células blancas de la sangre, los llamó “nucleína”. Sus hallazgos fueron publicados por primera vez en 1871, pero su importancia no fue reconocida en ese momento (Dahm, 2008). Miescher pudo aislar y caracterizar el ADN debido a su buena elección de las células para sus experimentos. Después de utilizar los leucocitos provenientes de la pus de vendajes uso espermatozoides de diferentes especies y ya que este tipo de células no se incrustan en un tejido o matriz extracelular, pueden purificarse fácilmente especialmente en los espermatozoides, los núcleos son grandes en comparación con el citoplasma, lo que facilita un enriquecimiento de componentes nucleares (Dahm, 2008). Por otra parte, los estudios realizados por Theodor Boveri, Walther Flemming, Walter Sutton, y Edmund B. Wilson revolucionaron los campos de la citología y genética y sentaron las bases de la citogenética. T. Boveri investigó el papel de los cromosomas y su importancia durante el desarrollo embrionario y como elementos importantes para la herencia. Sus trabajos con erizos de mar mostraron que era necesario que todos los cromosomas estuvieran presentes para que un desarrollo embrionario correcto tuviera lugar. Este descubrimiento fue parte importante de la teoría cromosómica de Sutton y Boveri (Maderspacher, 2008).Walther Flemming realizó estudios detallados sobre la división celular en diferentes órganos y organismos, principalmente del reino animal (Paweletz, 2001). Flemming describió además la morfología y el comportamiento de los cromosomas durante la mitosis, acuñando los términos “cromatina” y “mitosis” (Figura 2). A finales de los años 1880 y 1890, Boveri y Walter Sutton de manera independiente comenzaron a desarrollar la teoría cromosómica el cual dicta que los cromosomas llevan material genético y son la base de la herencia mendeliana (Dahm, 2008; Ramirez, Hulston, & Kovac, 2015).
Si bien la mayoría de estos descubrimientos y conceptos fueron bien recibidos por la comunidad científica en su momento, el descubrimiento del ADN por Friedrich Miescher fue poco apreciado, ya que la gran mayoría de los científicos de la época seguían convencidos de que las proteínas por su complejidad eran las portadoras de la información genética; y no fue sino hasta el siglo XX que se comprendió el verdadero significado de sus hallazgos.
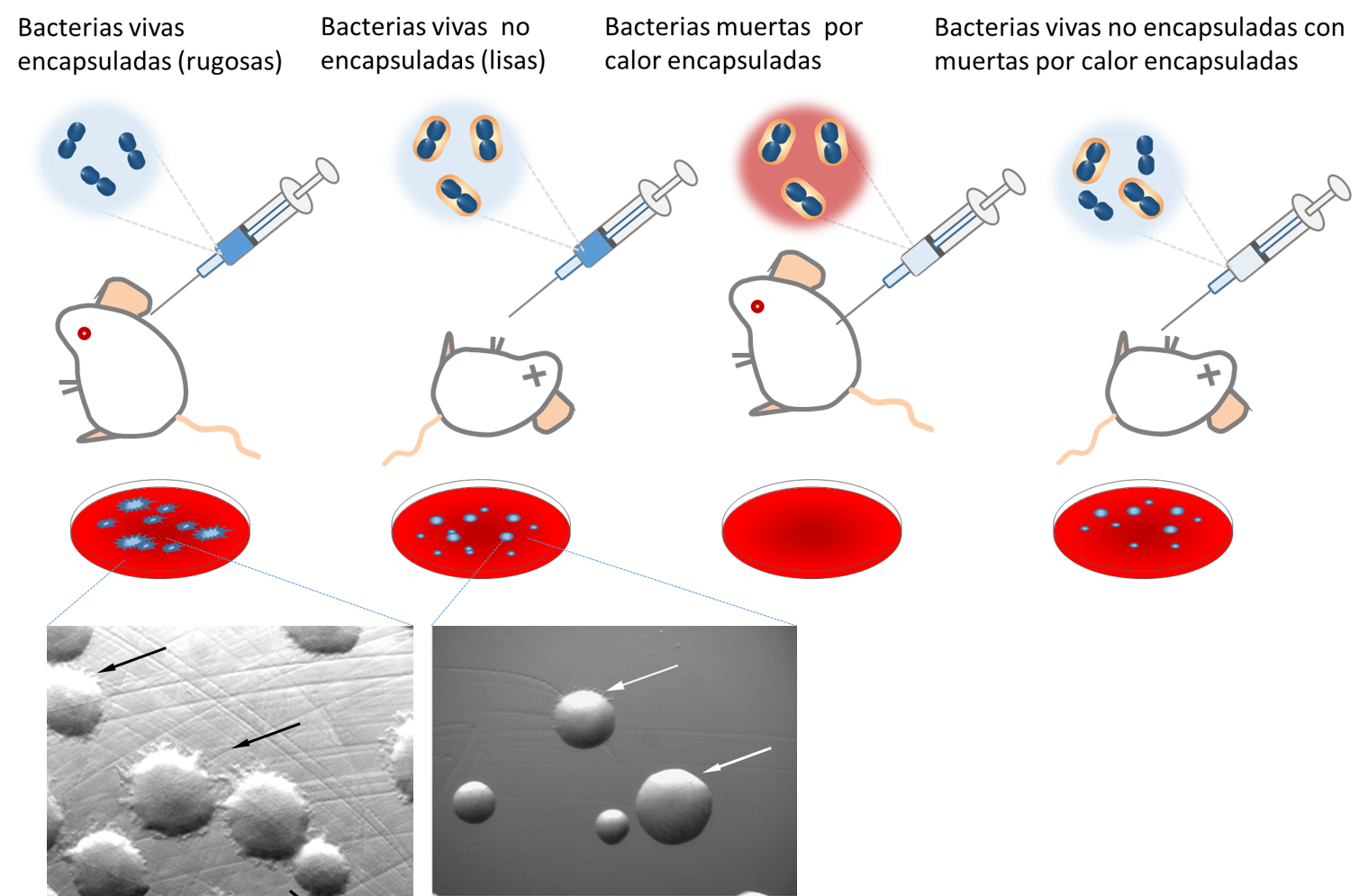
Uno de los científicos que se interesó por los trabajos de Miescher fue Albrecht Kossel un científico que trabajaba en el laboratorio de Hoppe-Seyler y que se interesó en las nucleínas como un nuevo elemento funcional de la célula. Posteriormente se hizo acreedor del Premio Nobel de Medicina en 1910 por descubrir la composición de la nucleína formado por cuatro bases nitrogenadas y moléculas de azúcar (Jones, 1953). En 1928, se llevó a cabo uno de los primeros experimentos que demostró el ADN podría transferir la información genética en un experimento en el cual, las bacterias eran capaces de transferir información mediante un proceso llamado transformación (figura 3). Frederick Griffith, que investigaba varias cepas de neumococo (Streptococcus pneumoniae), e inyectó dos tipos diferentes de cepas de neumococo a ratones; la cepa lisa (S) virulenta y la cepa rugosa (R) no virulenta. La cepa S es dañina, ya que se recubre de una capa de polisacárido que la protege del ataque del sistema inmune, mientras que la cepa R no produce esa cápsula protectora y es derrotada por el sistema inmune (figura 3). Griffith observó que, cuando la cepa S moría por calor no afectaba al ratón, pero cuando la combinaba con la cepa R y la cepa S muerta (por calor) la cepa R era de matar a su hospedero. Griffith llegó a la conclusión de que la cepa R se había “transformado” en una cepa S virulenta por un “principio de transformación” que de algún modo las baterías de la cepa S muertas virulentas transformaban a las bacterias R.
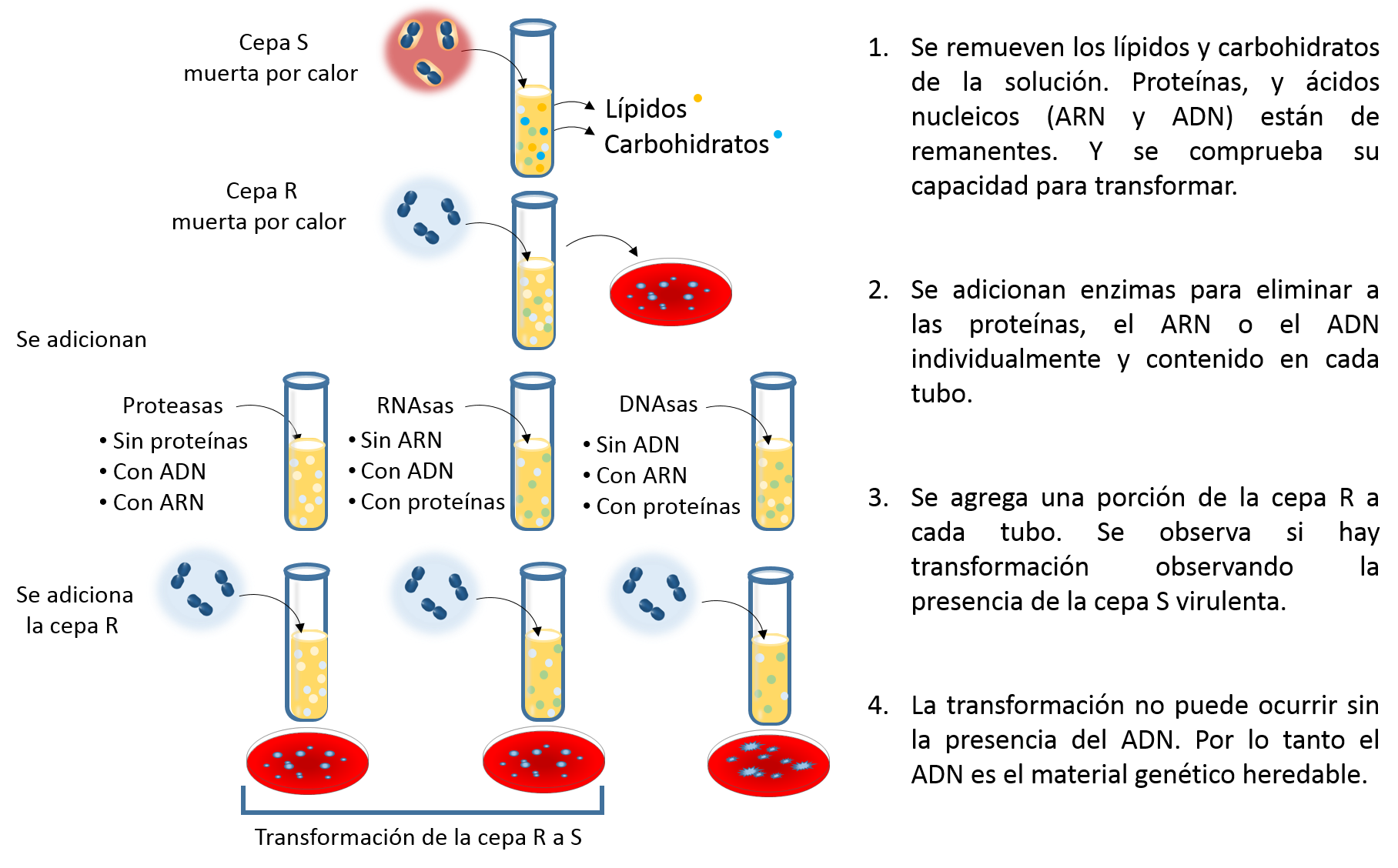
Este estudio se reavivó hasta a mediados de la década de 1940 y principios de 1950, cuando Oswald T. Avery, Colin MacLeod, McCarthy Maclyn, (figura 3) y por otra parte, Al Hershey y Martha Chase (figura 4) demostraron de manera independiente que el ADN es el portador de la información genética (Avery & Macleod, 1994; Hershey & Chase, 1952). Si bien la existencia del ADN se conocía desde 1869, en aquella época se creía que las proteínas eran las responsables en transmitir la información que determina la herencia. Avery, MacLeod y McCarty investigaron la naturaleza química del factor transformador, para determinar si era una proteína o un ácido nucleico. Basándose en los experimentos de Griffith, transformaron la cepa R en la cepa S incubando la cepa R viva y la S muerta por calor. Esto lo realizaron basado en un detallado y meticuloso experimento in vitro, realizando pretratamientos a los componentes celulares de la cepa S muerta por calor con diferentes enzimas que degradaban proteinas, ARN o ADN específicamente. Con estos experimentos pudieron concluir que el factor transformador era el ADN, ya que las enzimas rompieron selectivamente cada componente. En sus experimentos, Avery, MacLeod y McCarty encontraron que ni la proteasa, ni la rnasa afectaron la capacidad de la cepa S muerta por calor para transformar a la cepa R, únicamente la enzima DNasa (Figura 3).
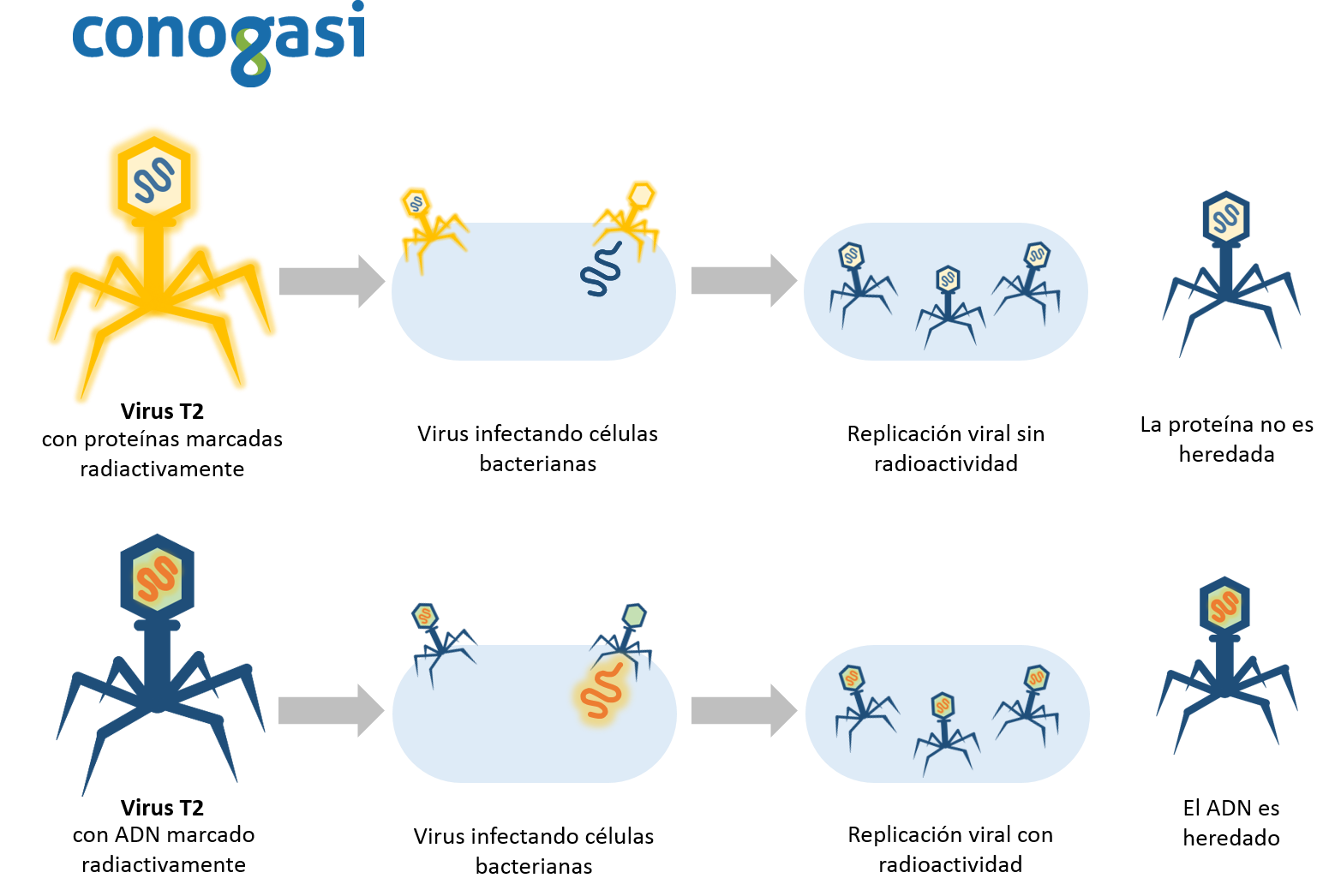
Independientemente, Alfred Hershey y Martha Chase realizaron una serie de experimentos para confirmar si el ADN o las proteínas son el material hereditario (figura 5). Hershey y Chase insertaron elementos radiactivos en los bacteriófagos (proteínas y ADN por separado). Cuando los bacteriófagos con el ADN marcado radioactivamente infectaron a las células bacterianas, las células nuevas contenían el material radiactivo en sus estructuras. Así mismo, cuando los bacteriófagos con las proteínas marcadas radioactivamente infectaron a las células, las bacterias nuevas no estaban marcadas. Por lo tanto, el experimento Hershey-Chase, concluyó que el ADN, es el material genético hereditario. En 1953 Watson y Crick usando los resultados de Rosalind Franklin sin su consentimiento (que estaban por publicarse) proporcionados de manera desleal por Wilkins, consiguen descifrar y dan la primera visión “teórica” de la estructura molecular del ADN (Watson & Crick, 1953).
En el mismo volumen de la revista Nature, Rosalind Franklin y Wilkins de manera independiente reportar estructuras cristalográficas del ADN proporcionado una primera visión experimental de su estructura y aspectos de su posible función (Franklin & Gosling, 1953; Wilkins, M.H.F., Stokes A.R., Wilson H.R, 1953). Una década más tarde, Robert W. Holley, Har Gobind Khorana, Marshall W. Nirenberg, y sus colegas consiguen descifrar el código genético (para más detalles consultar Articulo de Gen) (Singer, 1968). Con esta información se cimientan las bases para la genética molecular, la biología molecular y la biotecnología, ya que esta descifrar el código permite vislumbrar como a partir de una molécula compuesta de sólo cuatro diferentes bloques de construcción (A, T, C, G) es posible la riqueza y abundancia de vida en nuestro planeta.
Primeras aplicaciones del uso del perfil de ADN
Ciencias forenses
El perfil de ADN, es una técnica que analiza los atributos únicos del ADN de una persona. La aplicación de los perfiles de ADN ha revolucionado las pruebas de maternidad/paternidad, la medicina forense y la identificación de víctimas en desastres. El término “huellas dactilares de ADN” fue acuñado para aludir al uso tradicional de huellas dactilares como medio de identificación humana. Las huellas dactilares clásicas están sujetas a interpretación y las muestras utilizables pueden ser difíciles de obtener. Cuando se lleva a cabo correctamente, las pruebas basadas en el ADN no sólo proporcionan evidencia excluyente, sino que pueden proporcionar evidencia de la identidad de una persona sin sesgo. La primera prueba práctica de la huella dactilar del ADN, se realizó en 1983 e implicó una lucha de dos años por parte de Christiana Sarbah y su hijo, Andrew, para probar al Ministerio de Inglaterra que eran, madre de Andrew. Andrew llegó a Inglaterra después de una larga estancia en Ghana con su padre (separado de Christiana). Funcionarios de inmigración lo mantuvieron en el aeropuerto de Heathrow, alegando que su pasaporte era falso o que se había hecho una sustitución. Sólo después de un perfil de ADN se demostró su parentesco con Christiana Sarbah y se le permitió a Andrew permanecer en Londres.
En 1994, se creó el Proyecto Inocencia, tomando el caso de Marvin Lamont Anderson, condenado en 1983 por violación, secuestro, sodomía y robo en Virginia, basado casi en su totalidad en la identificación de la víctima. Anderson fue sentenciado a 210 años, aunque durante el juicio hubo evidencia de que otra persona pudo haber cometido el crimen. Anderson cumplió 15 años de su condena en la Penitenciaría del Estado de Virginia y cuatro años más en libertad condicional. Cuando el Proyecto Inocencia asumió el caso de Anderson, tuvieron dificultades para obtener la evidencia. La policía, el fiscal y la corte sostuvieron que el estuche de violación con la evidencia había sido destruido. En 2001, el Dr. Paul Ferrara, Director de la División de Ciencias Forenses de Virginia, localizó algunos hisopos del kit de violación que quedaron en el cuaderno de laboratorio del científico forense original asignado al caso de Anderson. Aunque el ADN se encontraba degradado era suficiente para producir un perfil de ADN con cuatro marcadores cortos de repetición en tándem (STR). El perfil STR de Anderson no coincidía mostrando que él no era el violador, y obteniendo su libertad (Innocence Project, 2017).
Perfil de ADN en medicina
La aplicación de la ciencia del ADN a la de alud y el bienestar humano está cambiando la investigación médica y clínica. Uno de las primeras investigaciones que destaco en el área científica fueron los hallazgos de Mary-Claire King una científica destacada de estado unidos se propuso buscar genes relacionados en el cáncer de mama. Se dedicó a recolectar datos de familias con una alta incidencia de cáncer de mama de inicio precoz. En 1990 King demostró que un solo gen del cromosoma 17, conocido como BRCA1, era responsable por varios cánceres de mamas y ovarios (entre un 5-10% de todos los casos de cáncer de mamas pueden ser hereditarios) (Hall et al., 1990). El descubrimiento del “gen del cáncer de mamas” revolucionó el estudio de muchas otras enfermedades, y modificó una posición general entre los científicos contraria a sus hipótesis sobre la existencia de una relación entre la genética y algunas enfermedades humanas complejas. La técnica desarrollada por la Dra. King para identificar el BRCA1 se ha probado con valiosos resultados para la detección del cáncer de mama y desde su descubrimiento se ha aplicado su técnica para el estudio de muchas otros tipos de cáncer como el ovárico, próstata (Barrois et al., 2004; Gallagher et al., 2010; Wooster & Weber, 2003).
Las aplicaciones del uso del ADN han tenido un gran impacto no solo en las ciencias médicas, sino también, en la biotecnología, farmacogenómica y en el estudio de la ancestria del humano y otros organismos. El desarrollo de métodos para su aislamiento y purificación hace posible su manipulación en el laboratorio como el uso de enzimas de restricción, la clonación de secuencias especificas o la amplificación mediante métodos como la PCR. Además, se puede generar secuencias de ADN artificiales e insertarlas dentro de plásmidos en otros organismos o mediante biobalística o vectores virales, entre otros (ver métodos biología molecular) (Sambrook, Fritsch, & Maniatis, 1989). Los organismos generados con estas técnicas sirven para producir generalmente proteínas recombinantes u otras biomoléculas de interés. El uso intensivo del ADN es de suma importancia para las investigaciones en biología molecular, agricultura y ganadería además de la biomedicina (Daniell & Dhingra, 2002; Houdebine, 2007; Liu, Yuan, & Stewart Jr, 2013).
Recientemente, la revolución genómica (el estudio de todo el material genético: ADN dentro de una célula, tejido u organismo) ha catapultado a la biología molecular en el campo de la biología de sistemas. Estas dos líneas de investigación han convergido para formar la biología de sistemas contemporánea. La biología de sistemas implica el modelado matemático de sistemas biológicos complejos. Uno de los objetivos de la biología de sistemas es modelar y descubrir propiedades emergentes en células, tejidos y organismos cuya descripción teórica sólo es posible en el ámbito de competencia de la biología de sistemas. En la última década, este campo se ha desarrollado rápidamente y aunque se han estado describiendo sistemas cada vez más complejos, realizar una descripción completa es mucho más importante que simplemente agregar componentes adicionales a un modelo. La posibilidad de realizar este tipo de estudios (descripciones completas) causará un cambio tanto en el paradigma teórico como a nivel experimental (Snoep & Westerhoff, 2005). En organismos unicelulares (levaduras y bacterias) y líneas celulares bien definidas de organismos superiores (humano, ratón, etc.), los enfoques de sistemas están dando pasos importantes hacia aplicaciones en biotecnológicas (Westerhoff & Palsson, 2004).
Biología de sistemas en cáncer
La biología de sistemas en el estudio del cáncer es un ejemplo del enfoque de biología de sistemas. Se trabaja con los datos específicos como datos genéticos y epigenéticos, además se analizan las redes de interacción intracelular y extracelular (Masoudi-Nejad et al., 2015) provenientes de líneas celulares de cáncer, modelos de ratón y muestras de pacientes.
Uno de los objetivos principales que persigue la biología de sistemas en cáncer es mejorar el diagnóstico, mejorar su clasificación y predecir los resultados de un tratamiento específico, que son las bases para una medicina personalizada (Butcher, Berg, & Kunkel, 2004). Aunque los modelos moleculares de la función de las células y tejidos humanos son aún un objetivo distante, los esfuerzos de biología de sistemas ya están influyendo en el descubrimiento de fármacos (Butcher et al., 2004).
Se ha propuesto poner un mayor énfasis en los fármacos multicomponentes los cuales son un estándar en la quimioterapia, y su desarrollo ha requerido pruebas empíricas arduas. La aplicación de modelos matemáticos con validación experimental ayudan a la formulación de nuevas terapias, particularmente aquellas adaptadas a las necesidades específicas de cada paciente (Butcher et al., 2004; Fitzgerald, Schoeberl, Nielsen, & Sorger, 2006). Los análisis a gran escala de genes (transcriptomas), proteínas (proteomas) y metabolitos (metabolomas) conocidas como las ‘ómicas’; acelerarán dramáticamente la generación de hipótesis y se pondrán aprueba nuevos y mejores modelos del cáncer. Estas simulaciones por computadora ayudan a priorizar las metas para el diseño de ensayos clínicos. Los enfoques de biología de sistemas del cáncer son una promesa alentadora que podrá mejorar la toma de decisiones en el desarrollo farmacéutico (Butcher et al., 2004).
Cómo citar: Checa Rojas, A. (2017, 09 de Mayo ) ADN: Conceptos básicos y aplicaciones. Conogasi, Conocimiento para la vida. Fecha de consulta: Septiembre 18, 2025
Esta obra está disponible bajo una licencia de Creative Commons Reconocimiento-No Comercial Compartir Igual 4.0




Deja un comentario
Sé el primero en comentar!