En nuestro cuerpo existen una gran cantidad de proteínas, las que constituyen aproximadamente el 45 % de nuestro cuerpo (descontando el agua). Algunas de ellas, como son las proteínas musculares, forman parte esencial de la estructura de nuestro cuerpo. Otras realizan una gran cantidad de funciones, entre ellas está la regulación de nuestro crecimiento, de nuestra actividad metabólica, transporte de oxígeno, reparación de tejidos, e incluso la protección contra virus y bacterias patógenas. Una gran cantidad de padecimientos son provocados por la falta de la actividad de alguna proteína, como es el caso de la diabetes, la anemia crónica, inmunodeficiencias congénitas, hemofilia, o retrasos en el crecimiento. Esto fue reconocido por los científicos hace mucho tiempo, cuando se descubrió que la deficiencia de proteínas como la hormona de crecimiento o la insulina provocan enanismo o diabetes, respectivamente. El primer intento terapéutico para resolver es
tas enfermedades fue el recuperar estas proteínas de órganos de animales y humanos. En el primer caso, las proteínas obtenidas no son idénticas a las humanas, y en ambos casos sólo se obtenía una muy baja cantidad de proteína a costos extraordinariamente altos. En consecuencia, no era posible contar con la calidad ni cantidad de material suficiente para tratar las enfermedades. Además, estas fuentes presentan riesgos importantes, como la presencia de proteínas y virus contaminantes que pueden poner en riesgo la salud del paciente.
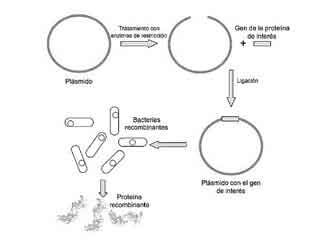
El descubrimiento de que el ADN contiene la información necesaria para la síntesis de proteínas abrió la posibilidad de producir proteínas muy similares a las humanas en microorganismos sencillos, como bacterias y levaduras, pero sin los problemas y riesgos de otras fuentes. El procedimiento consiste en introducir el ADN que contiene la información correspondiente a una proteína humana en particular en células del microorganismo productor. Esto se hace utilizando un plásmido, que es un pedazo de ADN circular que puede transferirse de un organismo a otro y que contiene varios elementos necesarios para su permanencia en la célula y la producción de la proteína de interés. De esta forma, el microorganismo produce la proteína humana, además de sus proteínas, convirtiéndose en una “fabrica celular”.
Las proteínas producidas de esta forma son llamadas proteínas recombinantes.
La primer proteína recombinante aprobada para ser utilizada como medicamento en humanos fue la insulina, en 1982. Antes de estar disponible mundialmente la insulina recombinante, la diabetes se trataba con insulina extraída de páncreas de cerdos o bovinos, la que no es idéntica a la humana, lo que puede resultar en rechazo o neutralización de la proteína y una deficiente acción terapéutica. Además, la extracción de tejido animal puede resultar en contaminación con virus u otras substancias indeseables. El uso de la insulina humana recombinante evita estos problemas. Actualmente, el mercado mundial de la insulina recombinante está alrededor de los 7,000 millones de dólares al año.
Otro ejemplo es la hormona de crecimiento humana, la que anteriormente se recuperaba de cadáveres humanos y actualmente se produce de forma recombinante en bacterias, células de animales o levaduras. Un ejemplo interesante es el Factor VIII, el que es un factor esencial en la cascada de coagulación de la sangre, y que es deficiente en algunos
pacientes hemofílicos. La extracción del Factor VIII de sangre humana y su uso para tratar la hemofilia antes de los 1990s resultó en la transmisión del virus de la inmunodeficiencia humana, o los virus de hepatitis B o C a muchos pacientes hemofílicos. La producción recombinante del Factor VIII permitió el tratamiento de la hemofilia sin correr riesgos de transmisión de enfermedades.
Desde 1982, se han aprobado más de 130 medicamentos basados en proteínas recombinantes, los que incluyen factores de coagulación para tratar la hemofilia, vacunas contra la hepatitis B y el virus de papiloma humano, anticoagulantes, hormonas (insulina, hormona de crecimiento, etc.), factores hematopoyéticos (que promueven la proliferación de células sanguíneas) para tratar anemias o neutropenias, interferones e interleucinas para tratar enfermedades infecciosas, artritis reumatoide, cáncer y esclerosis múltiple, entre otros.
Muchas de las proteínas recombinantes usadas como medicamentos no existen en la naturaleza, sino que han sido creadas en los laboratorios para poseer más de una función.
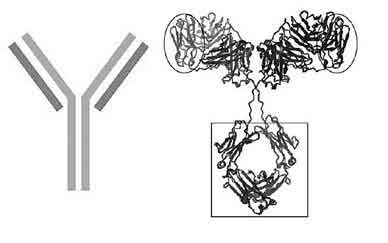
Recientemente han adquirido especial importancia los anticuerpos monoclonales recombinantes. Los anticuerpos forman parte del sistema de defensa de nuestro cuerpo. Son proteínas producidas por el sistema inmune cuando detecta alguna sustancia dañina, como virus, bacterias, hongos, parásitos o algunos químicos. Los anticuerpos tiene una región que une específicamente a la sustancia dañina (antígeno), y otra región que desencadena respuestas adicionales del sistema inmune. Con el fin de aprovechar las propiedades de los anticuerpos para el tratamiento de enfermedades, se han producido anticuerpos recombinantes a partir de un anticuerpo específico que reconoce una sustancia en particular.
Como se produce un sólo anticuerpo, se les llama anticuerpos monoclonales recombinantes. Algunos anticuerpos monoclonales recombinantes producen una respuesta inmune en nuestro organismo, mientras que otros neutralizan la acción de alguna molécula al unirse a ella. Los anticuerpos monoclonales se han utilizado para diagnóstico, para el tratamiento de cáncer, asma, y la artritis reumatoide, y para prevenir el rechazo de órganos transplantados, entre otras aplicaciones. Actualmente, un anticuerpo monoclonal, Etanercept, es el medicamento recombinante con mayor mercado en Estados Unidos, con ventas de aproximadamente 4,500 millones de dólares al año. El Etanercept se utiliza para tratar enfermedades autoinmunes al bloquear al factor de necrosis tumoral (TNF), molécula responsable de la respuesta inflamatoria. Es una proteína que no existe en la naturaleza, y que se generó al pegar dos segmentos de proteínas con funciones diferentes. Por un lado, contiene el receptor del TNF, el que le permite bloquear la respuesta inflamatoria, y por otro una porción de anticuerpo humano recombinante que le permite a la proteína permanecer por tiempos largos en el torrente sanguíneo. El Etanercept es un inmunodepresor que se utiliza para tratar la artritis reumatoide, la artritis juvenil y otras enfermedades similares.
Existen nuevos medicamentos en desarrollo basados en anticuerpos monoclonales recombinantes, como es el caso de un anticuerpo recombinante que está en pruebas clínicas para ser aprobado para el tratamiento de osteoporosis, pérdida de hueso y cáncer de hueso, entre otros. Se trata de un anticuerpo que bloquea un factor de remoción de hueso.
Millones de pacientes se han beneficiado con los nuevos medicamentos basados en proteínas recombinantes, muchos de ellos padecían enfermedades para las que no existía tratamiento hasta la aplicación de esta nueva tecnología. Además, la posibilidad de obtener grandes cantidades de proteínas humanas de forma recombinante ha permitido importantes avances en el área de la investigación, que se han traducido en muchos casos en los medicamentos que actualmente están en el mercado.
Las aplicaciones de la tecnología del ADN recombinante discutidas aquí son sólo algunos ejemplos de los beneficios que la tecnología del ADN recombinante ha aportado a la humanidad.
Cómo citar: Autor, C., Laura A. Palomares y Octavio Tonatiuh Ramírez (2018, 15 de Julio ) Las proteínas recombinantes: nuestras aliadas en la salud. Conogasi, Conocimiento para la vida. Fecha de consulta: Octubre 10, 2025
Esta obra está disponible bajo una licencia de Creative Commons Reconocimiento-No Comercial Compartir Igual 4.0




Deja un comentario
1 Comentario en "Las proteínas recombinantes: nuestras aliadas en la salud"
Interesante y útil muchas gracias. Si tuvieran más referencias sobre el nombre del anticuerpo monoclonado que bloquea un factor de remoción de hueso.
Gracias.