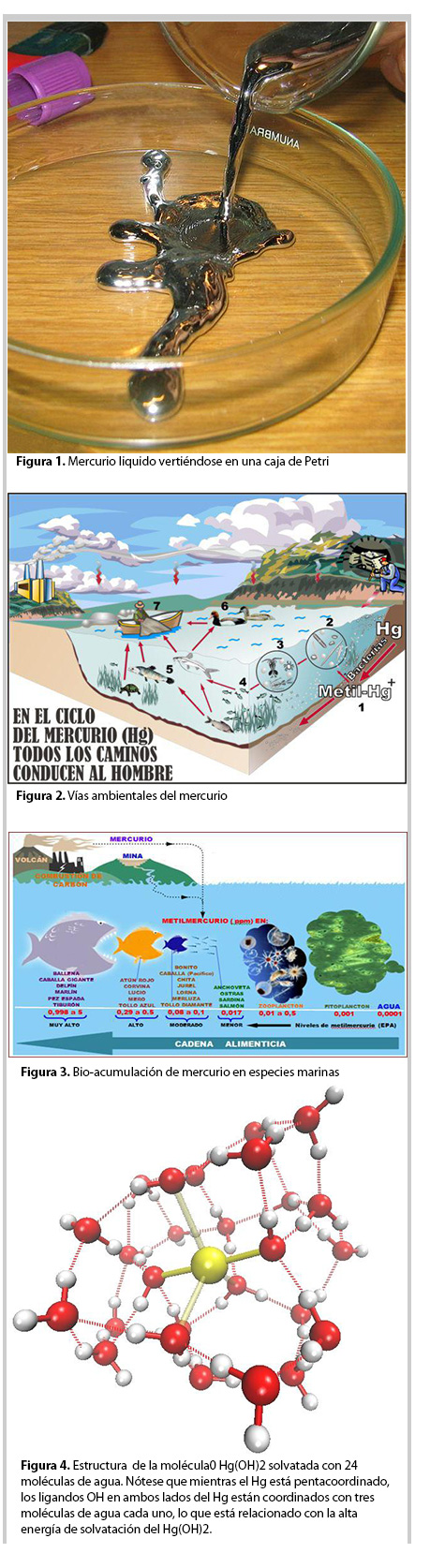
Es probable que alguna vez hayas tenido en tus manos un termómetro basado en mercurio; sin duda habrás apreciado con curiosidad y fascinación el peculiar líquido plateado que contienen dichos instrumentos de medición. En este artículo conoceremos más sobre las propiedades este elemento químico denominado mercurio y su impacto en el medio ambiente y la salud.
El mercurio es un elemento químico que se encuentra de forma natural en la corteza terrestre, en la atmósfera, la biósfera y la hidrósfera. El símbolo que se utiliza para representarlo es Hg y proviene de su antiguo nombre en griego hydrargyrum, que significa “plata acuosa“, en referencia al aspecto plateado del metal y a su estado líquido a temperatura ambiente (figura 1). Las propiedades físicoquímicas inusuales del mercurio provienen de su muy alto número atómico, Z=80 y de efectos de la teoría de relatividad. Estos efectos, descubiertos por Einstein, modifican sustancialmente las propiedades del tiempo y el espacio cuando los objetos viajan a muy altas velocidades. Dado que los humanos y nuestros dispositivos somos muy lentos respecto a la velocidad de la luz, los efectos relativistas no nos afectan ni los percibimos, pero, en cambio, son fundamentales para definir las propiedades de átomos y moléculas. Los efectos relativistas en el mercurio son enormes, ya que la fuerza de atracción hacia los 80 protones en su núcleo hacen que sus electrones más internos se muevan a una velocidad de 175,182 kilómetros por segundo (km/s), es decir, a una fracción apreciable 80/137 de la velocidad de la luz. Los efectos relativistas afectan la estructura electrónica del mercurio en su capa de valencia y conducen a un enlace químico entre átomos de mercurio tan débil que lo vuelve el único metal líquido a temperatura ambiente de toda la Tabla Periódica Durante más de veinte siglos el mercurio ha tenido diversas aplicaciones en diferentes culturas del mundo, principalmente a través de la fabricación de pinturas (bermellón), ungüentos médicos, amalgamas dentales, termostatos, barómetros, termómetros, lámparas de vapor y fluorescentes, baterías de larga duración, fungicidas y plaguicidas, e incluso fue usado en el tratamiento de enfermedades como la sífilis. Sin embargo, hay que hacer énfasis en que el mercurio es altamente tóxico. Cuando su concentración en algunos órganos supera cierto umbral produce un gran número de enfermedades en humanos y animales, algunas de ellas mortales. Desafortunadamente, las emisiones de mercurio a la atmósfera, procedentes de actividades humanas, han aumentado dramáticamente durante los últimos 150 años, debido primordialmente a la creciente industrialización global. Se estima que la cantidad total de Hg emitida a la atmósfera cada año, proveniente únicamente de las fuentes antropogénicas, es de alrededor de 2000 toneladas, así que no es sorprendente encontrar altos niveles de mercurio en suelos, sedimentos, ecosistemas acuáticos, y aun en zonas muy remotas como el ártico. La principal consecuencia de las emisiones no controladas de mercurio a nuestro medio ambiente es la bio-concentración en aves, mamíferos y, principalmente, en animales marinos. Estos últimos presentan, además, una tendencia natural de acumulación a través de las cadenas alimenticias. Especies superiores de la cadena tróficacomo el tiburón, el pez espada, la caballa, el atún, etc., contienen concentraciones más elevadas de mercurio que otras especies, al ser los principales depredadores del medio marino (figuras 2 y 3).
Un informe reciente del la organización de vigilancia sanitaria mundial sobre los niveles de mercurio en el medio ambiente, Mercury Police Project [2], establece que los niños sólo deben comer atún una o dos veces al mes para mantener su ingesta de mercurio en un nivel seguro y evitar los daños en las funciones cognitivas producidas por la ingesta de este metal pesado. El responsable de esa investigación emite una recomendación muy concreta a los padres de familia: los niños deben evitar comer atún blanco albacora, ya que contiene el triple de mercurio que el atún light. Más aun, niños con un peso mayor a 30 kg podrán ingerir atún light hasta dos veces al mes, pero aquellos con un peso menor, sólo una vez.
Por su toxicidad, el mercurio representa un riesgo constante para la salud de los seres vivos, incluidos los seres humanos. Para entender los mecanismos de acción del Hg, es indispensable saber cómo ingresa a las cadenas alimenticias. Dicho ingreso se inicia con el paso de alguna molécula estable que contiene Hg a través de la membrana celular de organismos inferiores acuáticos como bacterias, algas, fito y zooplancton. A la fecha se desconoce si este proceso ocurre por difusión o por procesos más complejos, como ocurre con las especies tóxicas de arsénico. En este contexto, resulta fundamental entender cómo se diluyen las especies moleculares más comunes que contienen Hg (HgCl2, HgClOH y HgOH2) en medios acuosos. Para responder en detalle a preguntas tales como ¿cuál especie requiere de más moléculas de agua para quedar totalmente envuelta por ellas? o ¿cuál especie se liga más fuertemente con el agua? En colaboración con investigadores del Instituto de Ciencias Físicas-UNAM en Cuernavaca y del Laboratoire de Physicochimie de Nano-Objets de la Universidad de Toulouse, Francia, estamos realizando un estudio sistemático del proceso de hidratación de las especies HgCl2, HgClOH y HgOH2 mediante cálculos de estructura electrónica. Este análisis permite comparar propiedades energéticas y estructurales para las diferentes especies conforme el número de moléculas de agua que rodean a estas moléculas metálicas se incrementa. Entre los resultados más importantes, encontramos que es necesaria la presencia de 24 moléculas de H2O para completar la primera capa de solvatación de HgCl2 y HgOH2, y que en ambos casos el Hg se encuentra coordinado con cinco átomos en simetría de bipirámide trigonal (figura 4). Nuestro resultado sugiere que el HgCl2 se despoja fácilmente de su entorno de agua cuando se acerca a la membrana celular, siendo ésta particularmente repelente al agua, como ocurre con el aceite. Puesto que el HgCl2 es una molécula neutra y no polar, se difunde fácilmente a través de la membrana celular, atravesándola con una velocidad 20 veces mayor que la del agua [4]. Hemos descubierto que las especies que contienen grupos hidroxilo (OH) se rodean más fácilmente con moléculas de agua e interaccionan más fuertemente con ella que las que no los tienen. Esto sugiere que el HgCl2 es la especie mercúrica responsable del transporte de este metal al interior de la célula. De esta forma, nuestros estudios explican a nivel molecular por qué el HgClOH es más lento que el HgCl2 y por qué el Hg(OH)2 es aún más lento que HgClOH en atravesar la membrana celular, resultados importantes para entender la acción tóxica del mercurio.
Artículo publicado originalmente “El Mercurio: elemento fascinante y mortal” en el periódico Unión de Morelos por miembros de la Academia de Ciencias de Morelos A.C.
Cómo citar: Autor, C., Jorge Iván Amaro Estradaa y Alejandro Ramírez Solísb aEstudiante del Doctorado en Ciencias, Facultad de Ciencias, UAEM. bDepto. de Física, Facultad de Ciencias Universidad del Estado de Morelos Miembro de la Academia de Ciencias de Morelos (2018, 21 de Septiembre ) El Mercurio: Elemento fascinante y mortal. Conogasi, Conocimiento para la vida. Fecha de consulta: Septiembre 17, 2025
Esta obra está disponible bajo una licencia de Creative Commons Reconocimiento-No Comercial Compartir Igual 4.0




Deja un comentario
Sé el primero en comentar!